过氧化氢
浏览: 4
导读:过氧化氢 : H2O2[1]又称双氧水、Albone、Hioxyl。自然界仅微量存在于雨雪中。纯者为无色透明液体。无嗅(或略有特殊气味)。有苦味。相对分子质量34.02。相对密度1.4649。熔点-0.89℃,凝固时为白色晶体。沸点151.4℃。折射率1.4067(25℃)。不溶于石油醚,溶于乙醇和乙醚,与水可任意混溶。市售品浓度为3%~90%,多数为30%,3%者相
过氧化氢 :
H2O2 [1]
又称双 氧水、Albone、Hioxyl。自然界仅微量 存在于雨雪中。纯者为无色透明液体。 无嗅(或略有特殊气味)。有苦味。相对 分子质量34.02。相对密度1.4649。熔点 -0.89℃,凝固时为白色晶体。沸点151.4℃。 折射率1.4067(25℃)。不溶于石油醚,溶于乙醇 和乙醚,与水可任意混溶。市售品浓度为 3%~90%,多数为30%,3%者相对密度1.00, 折射率1.3350;30%者相对密度1.132,沸点 107℃;50%者相对密度1.196,沸点111.0℃;60% 者相对密度1.241,沸点120℃,90%者相对密度 1.438,沸点150℃。过氧化氢分子中有过氧 键(—O—O—),氧原子的氧化态为-1,介于0 和-2之间,所以它既有氧化性,又有还原性,但 以氧化性为主,只有在强氧化剂存在时,才表现 为还原性,本身被氧化,并放出氧。
2KMnO4+5H2O2+3H2SO4→
2MnSO4+K2SO4+5O2+8H2O
Ba(OH)2+H2O2→BaO2+2H2O
当过氧化氢浓度较高(65%以上)时,与有机物 接触,可分解,光、热及金属离子可促进分解,分 解后产生氧,并可发生爆炸、放出大量的热。
2H2O2→2H2O+O2+196kJ
用途: 用作漂白剂、杀菌剂、氧化剂、脱氯 剂;火箭燃料;制造过氧化物的原料;寒冷地区小 麦和稻谷发芽的助剂;除铁剂;橡胶制品的添加 剂;化妆品添加剂;整容剂(防皱);医疗时伤口的 消毒剂;食品方面用作漂白剂、氧化剂、淀粉改 性剂和防腐剂;纸塑无菌包装时,包装前的包装 材料消毒剂;鱼子的漂白,然后用过氧化氢酶将 剩余过氧化氢分解,不使其残留,因过氧化氢可 破坏维生素C。
制法: ①硫酸与过氧化钡反应,可制 得[1]。
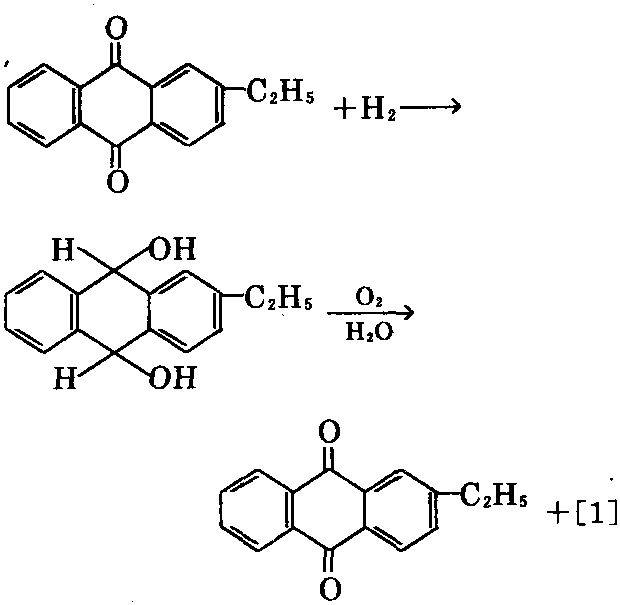
② 由2-乙基蒽醌在钯催化剂作用下加 氢,制得氢化蒽醌,进一步用空气氧化,可制 得[1]。2-乙基蒽醌可循环使用。
③ 电解酸性硫酸铵,生成过二硫酸铵,过 二硫酸铵进一步水解,生成[1]及酸性硫酸铵。 用水吸收过氧化氢,然后浓缩,可制得[1]。
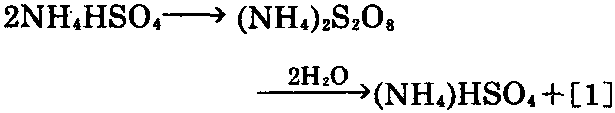
阴极:2H++2e→H2
阳极:2SO42--2e→S2O82-
 客服热线:
客服热线:


